Para os químicos, a cromatografia flash faz parte do fluxo de trabalho de síntese diário. Para a maioria das sínteses, as misturas de reação bruta são purificadas por cromatografia em fase normal (também conhecida como adsorção). No entanto, há momentos em que a complexidade e a polaridade da mistura bruta tornam a cromatografia em fase normal muito desafiadora. Para essas situações, a cromatografia em fase reversa (também conhecida como partição) pode ser uma opção preferida.
Mas, se você tiver apenas um sistema flash disponível, como alternar eficientemente de solventes de fase normal não polares para solventes de fase reversa polares – e vice-versa sem problemas? Você poderia ou deveria fazer isso? Neste post, tentarei esclarecer um pouco o assunto.
A mudança drástica de polaridade do solvente em um sistema cromatográfico é um processo evitado pela maioria dos químicos. Por quê? Porque existem temores de solventes residuais que podem interferir na próxima execução da cromatografia e há preocupações sobre o impacto de mudanças drásticas de polaridade nos componentes fluídicos do sistema, especialmente vedações da bomba e válvulas de retenção. Esses são problemas reais e, para a maioria dos laboratórios, eles preferem ter dois sistemas de flash – um para fase normal e outro dedicado à fase reversa, em vez de trocar solventes.
Embora os problemas sejam reais, você pode alternar eficientemente entre as fases normal e reversa apenas lavando / preparando o sistema com uma série de solventes miscíveis. Isso pode ser feito rapidamente, normalmente em menos de um minuto, sem afetar negativamente o sistema. Fiz isso várias vezes com o Biotage® SPx, Isolera e agora os sistemas Selekt com ótimos resultados e sem problemas de fluidos!
Para alternar de fase normal (hexano / acetato de etila) para fase reversa (metanol ou acetonitrila e água) – prepare o sistema (sem uma coluna anexada) com 50-100 mL de acetato de etila, depois metanol (ou acetonitrila) e água para os mesmos volumes.
Para passar da fase reversa para a fase normal, inicie com metanol (ou acetonitrila), seguido por acetato de etila e depois hexano, todos entre 50 e 100 mL.
Para a maioria dos sistemas de flash, a troca de solvente acima é uma operação manual. Com o novo sistema Selekt, esse processo agora é automatizado, o que é realmente conveniente. Ele é projetado com dois caminhos de fluxo independentes e, portanto, pode ser usado para cromatografia em fase normal e em fase reversa. O sistema entende que a água é um solvente de fase reversa; portanto, quando você programa um método de purificação em um dos dois canais com água como solvente, o sistema Selekt realiza automaticamente a troca de solvente por você. O mesmo acontece ao realizar uma purificação de fase normal após uma execução de fase reversa.
Esse é um recurso do sistema que eu acho mais benéfico, pois agora posso avaliar rapidamente se uma purificação é melhor executada por métodos em fase normal ou reversa sem interromper meu fluxo de trabalho para trocar manualmente os solventes.
Desculpe se isso soa como um discurso de vendas, mas não é para isso, mas quando encontro um produto verdadeiramente único e benéfico, gosto de compartilhar as informações.
Tive a oportunidade de testar esse recurso com uma reação que criou uma mistura muito confusa, Figura 1.
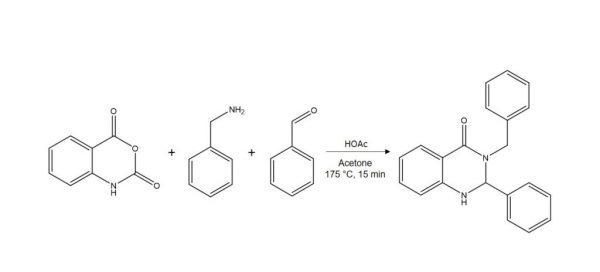
Figura 1. Reação de síntese em acetona a 175 ° C por 15 min.
A TLC em fase normal (2 placas) em 20% e 30% de EtOAc / hexano provou mais uma vez minhas limitações aparentes como químico orgânico (é por isso que pratico cromatografia!). Eu usei duas razões EtOAc / hexano para determinar qual fornece a melhor separação das duas misturas, a mistura de reação bruta e que eu sei que seria arriscada, mas forneceria informações sobre a complexidade e uma mistura de reação bruta diluída para simplificar a análise por TLC, Figura 2.

Figura 2. TLC da mistura de reação em 20% EtOAc / hexano (esquerda) e 30% EtOAc (direita). C = concentrado, D = mistura RxN diluída em DCM.
A partir dos dados da TLC, criei um gradiente segmentado no sistema Biotage® Selekt, que proporcionou uma excelente separação com uma coluna Biotage® Sfär de 10 gramas, 20 µm e uma carga de 90 mg, Figura 3.
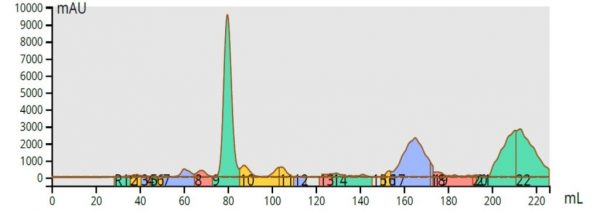
Figura 3. A purificação em fase normal da mistura de reação com acetona (carga de 90 mg) usando um gradiente segmentado fornece excelente cromatografia com o produto (grande pico azul) completamente resolvido a partir de sua impureza à direita.
No canal 2 do sistema Selekt, programei um gradiente de 50-100% de MeOH em fase reversa em água usando uma coluna flash de 12 gramas Biotage® SNAP Ultra C18. Depois de pressionar o botão play, o sistema Selekt lavou a tubulação interna com os solventes necessários a 300 mL / min e começou automaticamente a equilibrar a coluna C18. A cromatografia resultante de uma carga idêntica de 90 mg foi bastante boa, embora eu não tenha otimizado o gradiente, Figura 4.
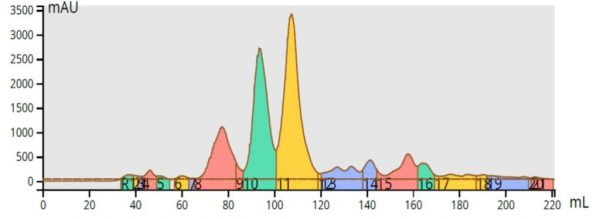
Figura 4. A purificação em fase reversa da mistura de reação (carga de 90 mg) mostra uma boa separação usando um método não otimizado. O produto é o pico verde.
Então, você pode trocar os solventes do seu sistema flash para realizar a cromatografia flash em fase normal e reversa? Na minha experiência, você deveria.

